
【政策解读】卫健委一天连发两项通知 新冠防控又有新规

目前由于各医疗机构要对发热门诊、新入院患者数及其陪护人员,普通门急诊就诊患者和“愿检尽检”人群进行新冠检测,随着检测目标人群的扩大和门诊患者量的进一步恢复,医院每日需要检测的人群数量迅速增加,因此检测能力亟待提升。而检测能力的提升,一方面是设备通量增大,一方面是专业的核酸检测人员增加。这对于检测任务已经十分繁重,人手紧缺的检验科来说,面临严峻考验。

4~6小时的检测结果报告时间将会是今后医院机构新冠核酸检测的基本要求,尤其面对危重症患者,如何能最大程度缩短检测时间,将是医疗机构重点关注的。

此点要求与2010年发布的《医疗机构临床基因扩增检验实验室管理办法》卫办医政发〔2010〕194 号文件内容一致,体现了对全自动一体机应用的认可,这项规范对于检验科场地局促的一些医院,以及门急诊等场地开展检测非常适合。


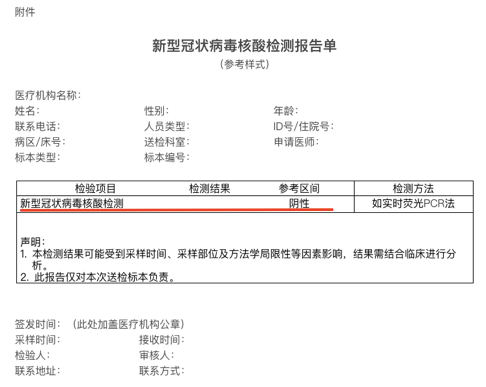
要求使用获得NMPA注册证的试剂,检测结果参考各试剂盒使用说明书的要求来判定,未对检测靶点数进行限制,在报告中只体现最终结果的阳性或阴性。强调了各医疗机构之间应做到检测结果互通互认,不再因各试剂厂家的要求不同而需重新检测。

优势一:快速,高通量
采用流水线作业模式,实现了核酸检测如同生化免疫一样,样本采集后原管上机,随到随检,90分钟报告第一个结果,之后连续出报告,平均2分钟自动报告一个结果,8小时200个检测,24小时700个检测。除了能满足当前政策对于4-6小时常规报告的时间要求,还能最大程度缩短急危重症患者检测时间。
优势二:占地面积小,环境要求低
AutoSAT集成了核酸提取、扩增检测、结果分析于一体,仅需一个房间,发热门诊即可检测,真正实现从就诊、取样、检测封闭化。对于不具备检测能力的医疗机构,大大简化了实验室建设环节,自行开展核酸检测,保障出报告时间。
优势三:全自动,省人工
自动化程度高,只需要单人操作,简单易学,极大地减少检验人员工作量。
优势四:结果更准确
采用专利的特异性靶标捕获磁珠提技术,只提取新冠病毒RNA,排除其他核酸或杂质的干扰。再通过实时荧光恒温扩增检测技术,反转录和扩增同步进行,扩增速度得到极大的提高,对病毒载量低的样本也能快速捕捉到扩增信号,提高灵敏度。配套全自动平台,排除了人为操作所会带来的误差,结果判读智能且标准。




 沪公网安备 31011502014243号
沪公网安备 31011502014243号