
顶刊鉴析 | HBV RNA反映LLV患者病毒活跃状态
目前伴有低水平病毒血症(LLV)或既往低水平病毒血症(pre-LLV)的HBeAg阳性CHB患者的病毒转录和复制仍不清楚。山东大学第二医院王磊教授团队于本月发表在Journal of Viral Hepatitis上的一篇研究尝试比较HBV RNA在不同分组中的含量变化,揭示不同LLV组和MVR组之间病毒水平复制与转录的差异。
方法
这项横断面研究招募2023年4月1日到2023年8月31日在山东大学第二医院就诊的147名HBeAg阳性CHB患者,接受NA治疗48周以上,包括LLV组43名,前LLV 组25名,以及MVR组79名。LLV组定义为接受一线抗病毒药物治疗后HBV DNA含量处于20 IU/mL ~ 2000 IU/mL之间。前LLV(pre-LLV)组定义为有过LLV历史的CHB患者,在入组时已经达到HBV DNA低于检测下限(<20 IU/mL) 。MVR组定义为接受一线抗病毒药物治疗小于48周就实现了HBV DNA低于检测下限。HBV RNA的定量检测使用实时荧光恒温扩增检测技术(SAT)(上海仁度生物,LLQ 100 copies/mL)。
结果
病人接受ETV、TDF或TAF治疗,中位持续时间为58个月。HBV RNA的中位数为:LLV组为6.9拷贝/mL,LLV前组为6.1拷贝/mL,MVR组为3.8拷贝/mL。与MVR组相比,LLV组的患者抗病毒治疗持续时间较短,HBsAg、HBeAg定量和HBV RNA水平较高。同样,pre-LLV患者也表现出HBeAg水平和HBV RNA定量升高。进行PSM分析以调整组间的基线特征。值得一提的是,MVR组中HBV RNA的水平显著低于LLV组(P<0.01);同样,MVR组中HBV RNA的水平显著低于pre-LLV组(P<0.01)。
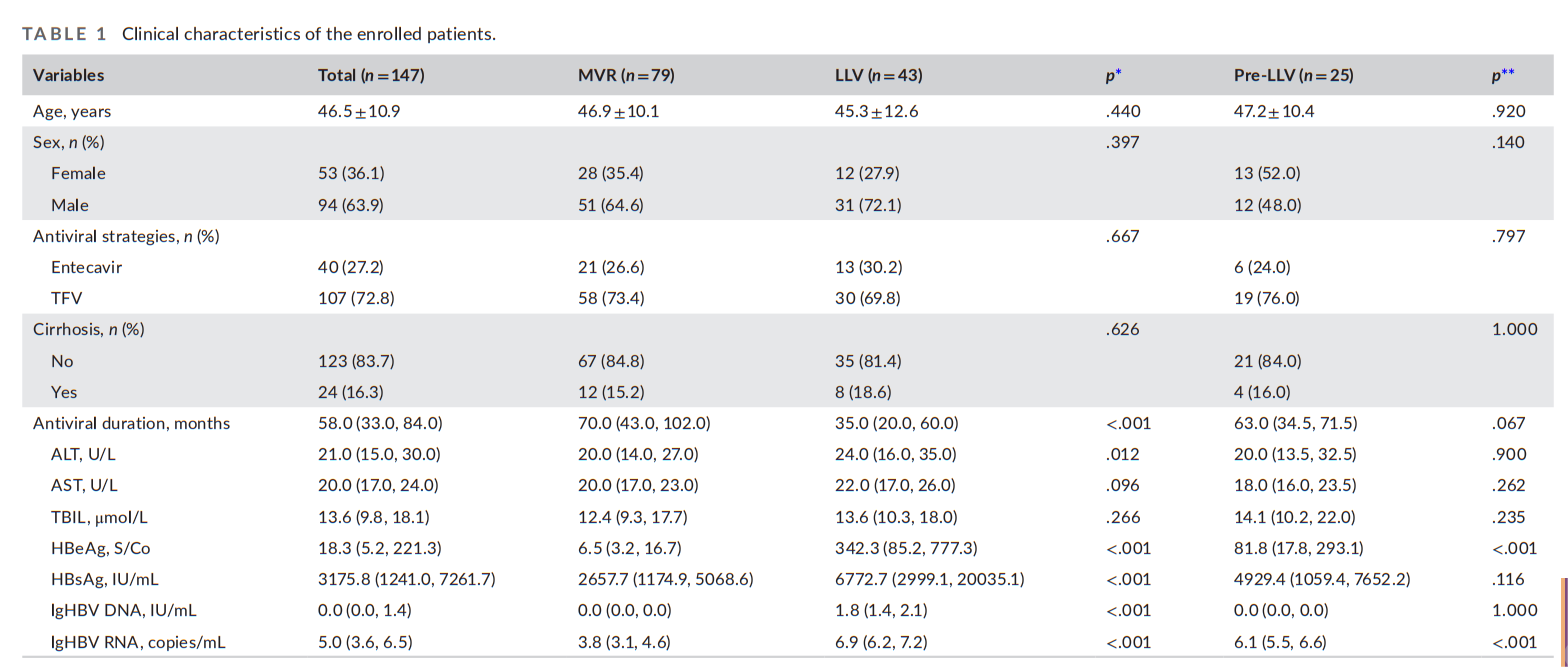
表1:入组患者的临床数据
结论
LLV和pre-LLV患者的HBV RNA水平均显著高于MVR患者,意味着不同LLV组和MVR组之间病毒水平复制与转录的差异。
仁度生物自主研发的乙型肝炎病毒核酸测定试剂盒,以其独特的检测技术、高灵敏性和高特异性等特点率先获准上市。区别于传统的PCR技术,本试剂盒采用独特的SAT技术,即RNA实时荧光恒温扩增扩增技术,能对RNA分子进行直接扩增和定量,不受样本中的HBV DNA干扰,无需DNA酶处理,检测下限低至50 copies/mL,搭载AutoSAT全自动平台,消除手工操作误差、节约实验室人力物力,为乙肝患者保驾护航。



 沪公网安备 31011502014243号
沪公网安备 31011502014243号